|
 |
- Search
| J Environ Anal Health Toxicol > Volume 23(2); 2020 > Article |
|
ABSTRACT
An analytical method to simultaneously determine 28 poly- and per-fluoroalkyl substances (PFASs), including PFASs alternative compounds (GenX, ADONA, and F53B) and precursors (N-MeFOSAA, N-EtFOSAA, 8:2FTUCA, 4:2FTS, 6:2FTS, and 8:2FTS) in wastewater samples using solid phase extraction (SPE) and liquid chromatography-tandem mass spectrometry (LC-MS/MS) was developed. Both the Korean standard analytical method and its modified analytical method for persistent organic pollutants (POPs) were applied, and the results were validated. However, the modified analytical method for POPs demonstrated better precision and accuracy for short-chain PFAS (e.g., PFBA), long-chain PFAS (e.g., PFDS), and emerging PFASs (e.g., GenX and ADONA). The accuracy and precision of the modified method for the 28 target PFASs ranged from 51% to 111% and 60% to 8.77%, respectively, with method detection limits (MDLs) of 0.17-2.14 ng/L. The modified analytical method was applied to eight industrial wastewater samples, and to two sewage water samples; 14 PFAS compounds were detected with total concentrations of 128.4-13,810 ng/L.
과불화화합물(Per- and Polyfluoroalkyl Substances, PFASs)은 지방족 탄화수소(Aliphatic hydrocarbon)의 수소가 전체(접두사: per-) 또는 부분(poly-)이 불소(fluorine)로 치환되고 다양한 친수성 작용기가 부착된 유기불소계 화합물로 1950년대부터 계면활성제 및 표면 처리제, 소화제용품, 반도체 세척용제, 살충제, 보온재 등 다양한 산업적 용도로 사용되고 있다[1]. 그러나 과불화화합물은 탄소와 불소의 강한 공유결합으로 인해 환경 내에서 쉽게 분해되지 않는 특성을 가지고 있고, 환경 중 잔류성과 축적성으로 인해 생물체를 비롯한 여러 환경 매체에서 축적 및 검출되는 것으로 알려져 있다[2]. 특히 여러 과불화화합물질 중 PFOS (Perfluorooctane sulfonate) 및 PFOA (Perfluorooctanoic acid)의 경우 생식 및 발달, 간 및 신장 그리고 면역계와 관련한 생물과 인체 독성이 보고되었으며 이 외 다른 과불화화합물의 독성에 대한 우려도 제기되고 있다[3]. 따라서 2009년 PFOS 및 그 염 그리고 PFOS-F (perfluorooctane sulfonylfluoride)는 Annex B [4], PFOA 및 그 염 그리고 PFOA 관련 화합물은 2019년 Annex A로서 POPs (persistent organic pollutants) 물질로 지정되었고[5], PFHxS (perfluorohexane sulfonic acid) 및 그 염 그리고 PFHxS 관련 화합물은 2019년 Annex A에 포함할 것을 제안하였다[6]. 또한 유럽연합(EU)은 PFOS의 산 및 사용을 EC 850/2004 규정에 의해 제한하고 2020년에 ECHA (European Chemicals Agency)의 평가에 따라 PFOA의 제조 및 시장에서의 유통과 관련하여 규제 결정을 내렸다[7]. 미국 환경청(EPA)은 2018년부터 2022년까지 PFASs 관리 및 실천 계획을 발표하여 PFOA와 PFOS를 중심으로 기준을 마련하고 대체물질 관련 연구를 수행하고 있다[8]. 2020년 현재 수계 내 과불화화합물의 주요 오염원으로 알려진 산업 폐수에서의 규제 및 가이드라인은 없으나, 미국, 유럽, 호주 등의 국가에서는 먹는물에서 PFOS, PFOA, PFHxS 또는 총 과불화화합물 농도를 기준으로 권고치를 설정하여 관리하고 있다[9]. 우리나라는 지난 2018년, 낙동강 지표수를 원수로 사용하는 정수처리장 수돗물에서 PFHxS가 최대 454.2 ng/L까지 검출됨에 따라 2018년 7월 환경부에서 과불화화합물 3종(PFOS, PFOA, PFHxS)을 먹는물 수질감시항목으로 지정 하였으며[10], 배출원 관리를 위해 낙동강 수계 지역은 2018년 7월부터, 기타 지역은 2019년부터 과불화화합물 3종을 수질 오염물질 감시 항목으로 지정하여 관리하도록 했다.
따라서 과불화화합물을 생산하거나 사용하는 업체들은 아직 국내 외에서 규제대상으로 지정이 되지 않은 불화탄소 고리 숫자가 작은 short-chain PFSAs (polyand per-fluorinated sulfonic acids C4-C7) 및 PFCAs (poly- and per-fluorinated carboxylic acids, C4-C7) [11] 혹은 탄소수가 많은 long-chain PFSAs (C9, C10) 및 PFCAs (C9-C18)를 PFOS 및 PFOA 대신 사용하는 것으로 보고하고 있다[12]. 최근 연구에 따르면 perfluoroalkyl chain 에 산성 작용기가 부착된 에스테르계 과불화화합물인 PFECA (perfluoroalkyl ether carboxylic acids)나 PFESA(perfluoroalkyl ether sulfonic acids) 등을 대체제로서 개발 및 사용하고 있다[13]. 이 중 알려진 대표적 과불화화합물 대체제는 F53B (potassium salt of 6:2 chlorinated polyfluorinated ether sulfonate), GenX (ammonium salt of 2,3,3,3-tetrafluoro-2-(1,1,2,2,3,3,3-heptafluoropropoxy) propanoic acid), ADONA (ammonium 4,8-dioxa3H-perfluoro nonanoate) 등이며 산업 현장에서 사용되고 있을 뿐 아니라 수환경 시료에서도 지속적으로 검출되고 있다[14]. F53B의 경우 PFOS의 대체제로 1970년 후반 중국에서 처음 생산되어 2009년 중국에서 약 20-30 ton 사용된 것으로 추정된다[13]. F53B는 중국에서 하수처리장의 유입수 및 유출수에서 각각 43-78 μg/L, 65-112 μg/L로 검출되었으며 이는 PFOS의 유입수(평균: 74 μg/L) 및 유출수(54 μg/L)의 농도와 유사한 수준인 것으로 보고되었다[15]. GenX와 ADONA는 PFOA의 대체제로서 주로 미국, 네덜란드 등에서 생산되어 사용되는 것으로 알려져 있다. GenX는 non-target screening 분석을 통해 2010년 미국 하천수에서 처음 검출되었으며[16] 네덜란드에서는 GenX 생산 공장 근처 하천수에서 ND-812 ng/L(평균: 98.0 ng/L)의 농도로 PFOA(ND-12 ng/L, 평균 : 4.1 ng/L)보다 약 24배 높게 검출된 것이 보고되었다[17].
현재 국내에서는 수질에서의 14 종의 PFASs 분석을 위해 주로 WAX cartridge를 이용한 고체상 추출법(solid phase extraction, SPE)이 많이 사용되고 있으며 국내 잔류성유기오염물질 공정시험법도 이를 이용한 시험법을 제시하고 있다[18-20]. 그러나 계속해서 신종 과불화화합물이 환경 중에서 검출되는 사례가 발견됨에 따라 국내 수질환경에서도 과불화화합물 대체제를 비롯한 신종 과불화화합물이 검출될 가능성이 있으며, 이들을 함께 효율적으로 분석할 수 있는 전처리법이 요구된다. 그러나 아직 국내에서 신종 과불화화합물을 분석한 연구는 전무하며 신종 과불화화합물 분석을 위한 전처리법이나 공정시험법 역시 제안되지 않은 실정이다.
따라서 본 연구에서는 국내 ‘잔류성유기오염물질 공정시험법’과 선행연구에서 많이 사용되는 전처리법을 사용하여 수질 시료에서 신종 과불화화합물을 포함한 28종의 PFASs 분석 가능성을 평가하고 최적 전처리법을 확인하고자 하였다. 나아가 본 연구에서 확인된 최적의 전처리법을 실제 산업 폐수 시료에 적용시켜 신규 과불화화합물 검출 빈도 및 농도 수준을 함께 파악하고자 하였다.
국내 산업 폐수 시료 내 과불화화합물 관련 공정시험법은 ‘잔류성오염물질공정시험기준 폐수 시료 중 과불화합물 (PFCs) 시험기준-LC/MSMS (ES 10390.1)’에서 지정하고 있는 과불화화합물 14종 (PFCAs 8종, PFSA 3종, 전구체 3종) 대상 시험기준과 ‘수질오염공 정시험기준, 과불화화합물-액체크로마토그래피-텐덤질량 분석법 (ES 04506.1)에서 지정하고 있는 과불화화합물 14종(PFCAs 10종, PFSAs 4종) 대상 시험기준, 총 두가지를 산업폐수의 분석에 적용하고 있다 (Table 1). 본 연구에서는 신종 과불화화합물 3종과 전구체 5종, 가 지형구조(Branched, Br-)를 가지는 과불화화합물 2종, PFCA 11 종과 PFSA 7종까지 총 28종을 연구 대상 물질로 선정하였으며 세부 물질은 다음과 같다. Perfluorocarboxylic acid 11종(perfluorobutanoic acid; PFBA, perfluoropentanoic acid; PFPeA, perfluorohexanoic acid; PFHxA, perfluoroheptanoic acid; PFHpA, perfluorooctanoic acid; PFOA, perfluorononanoic acid; PFNA, perfluorodecanoic acid; PFDA, perfluoroundecanoic acid; PFUnDA, pefluorododecanoic acid; PFDoDA, perfluorotridecanoic acid; PFTrDA, perfluorotetradecanoic acid; PFTeDA), Perfluoroalkyl sulfonate 9종(perfluorobutane sulfonate; L-PFBS, perfluoropentane sulfonate; L-PFPeS, perfluorohexane sulfonate; L-PFHxS, br-PFHxS, perfluoroheptane sulfonate; L-PFHpS, perfluorooctane sulfonate; L-PFOS, br-PFOS, perfluorononane sulfonate; L-PFNS, perfluorodecane sulfonate; L-PFDS), 과불화화합물 전구체 5종 (N-methylperfluoro-1-octane sulfonamidoacetic acid; N-MeFOSAA, N-ethylperfluoro-1-octanesulfonamidoacetic acid; N-EtFOSAA, 1H,1H,2H,2H-perfluoro hexanesulfonate; 4:2FTS, 1H,1H,2H,2H-perfluorooctanesulfonate; 6:2FTS, 1H,1H,2H,2H-perfluorodecabesulfonate; 8:2FTS), 신종 과불화화합물 3종(Dodecafluoro-3H-4,8-dioxanonanoate; ADONA, 2,3,3,3-Tetrafluoro-2-(1,1,2,2,3,3,3-heptafluoropropoxy)-propanoic acid; HFPO-DA (trade name: GenX), 9-chlorohexadecafluoro-3-oxanonane sulfonate; 9Cl-PF3ONS (trade name: F53B))이다.
본 연구에 사용된 모든 시약은 분석대상물질의 측정 분석 시 불순물에 의한 영향이 미치지 않는 것을 사용하였으며 모든 표준물질은 Wellington Laboratories (Guelph, ON, Canada)로부터 구매하였다. 표준물질 PFBA, PFPeA, PFHxA, PFHpA, PFOA, PFNA, PFDA, PFUnDA, PFDoDA, PFTrDA, L-PFBS, L-PFPeS, PFHxSK, L-PFHpS, PFOSK, L-PFNS, L-PFDS, N-MeFOSAA, N-EtFOSAA, FOSA, 4:2FTS, 6:2FTS 및 8:2FTS는 2μg/ml 농도의 혼합물질로 만들어진 PFAC-24PAR을 구입 후 희석하여 사용하였다. 내부표준물질은 (Internal standard, ISTD) perfluoro-n-[1,2-13C2] hexanoic acid (MPFHxA), perfluoro-n-[1,2,3,4-13C4] octanoic acid (MPFOA), perfluoro-n-[1,2,3,4,5-13C5] nonanoic acid (MPFNA), perfluoro-n-[1,2-13C2] decanoic acid (MPFDA), perfluoro-n-[1,2-13C2] undecanoic acid (MPFUnDA), perfluoro-n-[1,2-13C2] dodecanoic acid (MPFDoDA), sodium perfluoro 1-hexane[18O2] sulfonate (MPFHxS) 및 sodium perfluoro-1-[1,2,3,4-13C4] octane sulfonate (MPFOS)가 포함된 2 μg/ml 농도의 혼합물질로 만들어진 MPFAC-MXA을 구입 후 희석하여 사용하였다. ADONA, HFPO-DA (GenX), 및 9Cl-PF3ONS (major component of F53B)는 50 μg/ml 농도의 단일물질로 만들어진 시약을 구입 후 희석하여 사용하였다. 실린지 첨가용 내부표준물질(Recovery standard, RSTD)로는 13C8 치환체인 Perfluoro-n-[13C8]octanoic acid (M8PFOA) 및 sodium perfluoro-1-[13C8] octanesulfonate (M8PFOS)을 사용하였다. Milli-Q water, 메탄올 (methanol)은 B&J Honeywell(Morristown, NJ, USA)사의 HPLC 등급 이상의 용매를 사용하였으며, 암모늄아세테이트 (99%) 및 암모니아수는 각각 Wako (Osaka, Japan) and Junsei (Tokyo, Japan)사의 특급시약을 사용하였다. 시료의 정제 및 추출을 위한 카트리지로는 OASIS WAX (150 mg, 6 cm3; Waters, Milford, MA, USA)를 이용하였다. 시료의 정제 및 추출을 위한 고체상 추출(SPE; solid phase extraction)장치로는 Supelco (Bellefonte In, PA, USA)사의 VisiprepTM SPE Vacuum manifold를 사용하였다.
유리섬유여과지(GF/F, 0.45 μm, ∅47 mm, Whatman, Maidstone, UK)로 필터 된 지하수 시료 500 mL를 PP (polypropylene)병에 취하여 추출 전 내부표준물질 2.5 ng을 첨가하였다. 해당연구에서 28종의 과불화화합물은 내부표준법에 의해 분석되었으며 기기분석 전 실린지 첨가용 내부표준물질 2.5 ng을 첨가하였다.
본 연구에서는 기존 국내 폐수 시료 중 과불화화합물 분석 공정시험방법(전처리법 1)과 관련 문헌을 참고하여 추출 용매 조건을 수정 적용한 방법(전처리법 2)을 사용하여 28종 과불화화합물의 동시분석법을 개발하고자 하였다. 세부 전처리 방법은 Fig. 1에 나타내었으며 분석법의 비교 평가를 위해 대상 28종 PFASs를 함유하지 않은 것으로 예상되는 낙동강 상류 지역의 지하수 시료를 사용하여 실험하였으며, 대상 PFASs는 MDL 이하인 것을 확인하였다.
폐수 시료 중 과불화화합물(PFASs) 공정시험방법(ES 10390.1)에 따라 진행하였다[21]. SPE 장치에 WAX (150 mg, 6 cm3) 카트리지를 장착한 후 메탄올, Milli-Q water 각 4 mL를 차례로 통과시켜 컨디셔닝하였다. 이후 준비된 시료를 10-15 mL/min의 유속으로 카트리지에 통과시킨 후 12 mL의 증류수와 6 mL 메탄올 용액(20%)로 카트리지를 세척한다. 세척이 끝난 카트리지는 약 10분간 진공 감압펌프를 이용하여 건조한 다음 메탄올(0.1% 암모니아 포함 용액) 5 mL로 두 번 용리시켰다. 이 용리액을 질소농축기를 사용하여 0.5 mL 이하로 농축시켜 0.45 μm PP 실린지 필터로 여과시킨 후 실린지 첨가용 내부표준물질 첨가 후 최종 부피를 0.5 mL가 되도록 하였다.
Taniyasu et al. (2005)의 전처리법을 참고하여 공정 시험방법의 전처리 방법을 수정하여 진행하였다. WAX (150 mg, 6 cm3) 카트리지에 메탄올(0.1% 암모니아 포함 용액), 메탄올, Milli-Q water 각 4 mL를 차례로 통과시켜 컨디셔닝하였다. 이후 준비된 시료를 10~ 15 mL/min의 유속으로 카트리지를 통과시킨 후 4 mL의 25 mM 암모늄아세테이트 용액으로 카트리지를 세척한다. 세척이 끝난 카트리지는 약 20분간 진공 감압 펌프를 이용하여 건조한 다음 메탄올(0.1% 암모니아 포함 용액) 4 mL, 순수 메탄올 4 mL를 차례로 통과시켜 용리하였다. 이 용리액을 질소농축기(Turbo vap LV, Caliper life sciences, Hopkinton, USA)를 사용하여 0.5 mL 이하로 농축시켜 0.45 μm 실린지 필터로 여과시킨 후 실린지 첨가용 내부표준물질 첨가 후 최종 부피를 0.5 mL가 되도록 하였다.
기기분석에는 액체크로마토그래프-텐덤질량분석기(LCMS/MS)를 이용하였으며, Agilent사의 6460 triple quadrupole mass spectrometer를 검출기로 사용하였다. 컬럼은 4.6mm × 150mm, 3.5 µm pore size의 ZORBAX Eclipse XDB-C18을 사용하였다. 이동상은 메탄올을 용매 A로, 2mM 암모늄 아세테이트를 용매 B로 하여 gradient program을 사용하여 분석하였다. 이온화는 전자분무이온화 (Electrospray ionization, ESI) 방법을 사용하였으며 각 대상물질에 대한 전구이온(precursor ion, PI)과 정량/정성이온(quantification/qualification ion, QI 1/QI 2)을 각각 선정하여 다중 반응 모니터링(multiple reaction monitoring, MRM)으로 분석하였다. 자세한 기기분석조건을 다음 Table 1과 Table 2에 나타내었다.
두 종류의 전처리 방법을 비교 평가하기 위해, 동일한 지하수 시료 500 mL에 2.5 ng의 28종 과불화화합물 표준물질과 8종의 내부표준물질을 첨가하여 선택된 전처리방법으로 3회 이상 반복 실험 및 분석하였다. 또한 기존 시료에 함유되어 있을 분석물질을 파악하기 위해 각 과정마다 실험에 사용된 것과 동일한 시료에 혼합 표준물질을 주입하지 않고 내부표준물질만 주입하여 바탕시료로 하였다. 그리고 각 단계마다 동일한 3개 시료에서 검출된 농도를 바탕시료에서 검출된 분석물질의 농도로 보정해주었다. 이에 대한 결과값을 이용하여 정확도(Accuracy) 및 정밀도(Precision)를 산정하였다. 정확도를 계산하기 위해 첨가시료에 대한 평균측정값(CAM)과 첨가하지 않은 시료의 평균 측정값 (CS)과의 차이를 첨가 농도 (CA)로 나누어준 후 100을 곱한, 상대백분율 (%) (Eq. 1), 정밀도는 정확도 산출시 도출된 측정결과로부터 아래 식과 같이 평균측정값(x ¯
Eq. 1. Equation for calculating accuracy (%)
Eq. 2. Equation for calculating precision (%)
또한 선택된 전처리 방법을 사용하여 방법검출한계 (Method detection limit, MDL)와 정량한계 (Limit of quantification, LOQ)를 국내 잔류성유기오염물질 공정시험법에 따라 산정하였다. 지하수 수질 시료 500 mL에 2.5 ng의 혼합표준물질을 주입하여 7회 반복 분석한 결과의 표준편차에 각각 3.143배(자유도가 6[n-1]이고 99%의 신뢰구간에서의 student’s t-value), 10배를 하여 구하였다[21].
검정곡선은 내부표준물질 및 실린지 첨가용 내부표준물질이 포함된 39종의 대상 PFASs를 시료에서 검출되고 있는 농도범위와 MDL 수준을 고려하여 12단계의 농도범위(0.05, 0.1, 0.2, 0.5, 1, 2, 5, 10, 20, 50, 100, 200 ng/mL)로 제조한 혼합표준용액을 사용하여 작성하였다. 검정곡선의 상관계수(R2)는 모든 물질에서 0.99 이상으로 양호한 직선성을 보였다. 기기분석 전 메탄올을 기기에 주입하여 기기의 오염여부를 판단하였고 분석 대상 시료 10개당 1개의 바탕시료(field blank)와 검정곡선의 중간 농도범위인 표준용액(5.0 ng/mL)를 분석하여 실험 중 발생할 수 있는 오염과 기기분석 중 검정곡선의 변경여부를 확인하고자 했다. 시료 추출 전 내부표준물질을 시료에 주입하고 최종 주입한 실린지 첨가용 내부표준물질을 기준으로 내부표준물질의 양을 계산하여 회수율로 산정하였으며, 공정시험방법의 정도 보증, 정도관리 기준에 따라 내부표준물질의 상대감응 계수를 이용하여 계산하였다[20].
본 연구에서 확립된 28종 PFASs 분석법을 실제 산업 폐수 시료에 적용하여 PFASs의 농도 수준 및 검출 빈도를 파악하였다. 분석을 위해 2018년 5월, 경상북도 산업단지에서 채취한 방류수 시료 8개와 하수처리장의 방류수 시료 2개를 채취하였다. 시료는 PFASs 오염을 최소화하기 위해 PE병에 채수하였고, 모든 채수된 시료용기는 아이스팩과 함께 아이스박스에 담아 실험실로 이송한 후 분석 직전까지 −20°C에서 냉동 보관하였다. 모든 분석은 본 연구에서 확인된 결과를 토대로 채취된 시료를 method 2를 사용하여 추출하였고 작성한 검량곡선을 통해 PFASs를 정량하였다. 시료의 농도계산 시 방법검출한계 미만의 경우에는 모두 불검출(Not detected, ND)로 처리하였다.
기존 국내 과불화화합물 분석 공정 방법인 20% 메탄올을 세척용매로 사용한 방법(method 1)과 25 mM 암모늄 아세테이트를 이용한 방법(method 2)을 수질 시료에 적용하고 3회 반복하여 얻은 내부표준물질 8 종의 회수율 결과를 Fig. 2에 나타내었다. 수질 시료를 method 1로 전처리한 경우 평균 57.2-106.0%의 회수율을 보였으며 이때의 상대표준편차는 0.5-6.6%로 나타났다. 또한 수질 시료를 method 2의 과정을 거쳐 전처리한 경우 평균 62.3-102.9%의 회수율을 보였으며 상대 표준편차는 0.2-5.3%로 나타나 method 1과 유사한 회수율을 가지는 것으로 확인되었다. 이러한 결과는 US EPA [22]와 국내 잔류성 유기오염물질 공정시험법에서 제시한 회수율 허용범위인 50-150%, 60-120% (MPFUnDA, MPFDoDA: 40-120%)를 모두 만족하는 것으로 확인되었다. 하지만 두 전처리방법의 평균 회수율을 상호 비교하였을 때, 대부분의 내부표준물질은 유사한 값을 보였으나, method 2로 전처리 한 경우 MPFBA의 평균 회수율은 80.8%로 method 1의 72.7%보다 높았으며, MPFDoDA 또한 method 2가 method 1에 비해 약 5.1% 높은 회수율을 보였다.
각 전처리법을 대상으로 28종 과불화화합물 혼합 표준물질을 2.5 ng 주입하여 각 전처리방법의 유효성을 검토하였다 (Table 3). Method 1을 이용하여 전처리한 시료의 경우, L-PFDS (39%)를 제외한 모든 물질이 해당 농도에서 62-114%의 정확도를 보였다. 또한 PFTeDA (12.8%), br-PFHxS (15.3%), GenX (19.8%)를 제외한 모든 물질이 국내 잔류성유기오염물질 공정시험법 기준인 10% 이내의 정밀도를 보였다. Method 2에 따라 전처리 한 시료의 경우, 모든 물질이 해당 농도에서 51-111%의 정확도를 보였으며 10% 이내의 정밀도를 보였다. 따라서 각 전처리법에 따른 회수율, 정확도 및 정밀도를 모두 고려하였을 때, 총 28종의 분석대상물질을 물시료에서 분석하기 위한 방법으로 method 2가 더 적절한 전처리법으로 판단되었다.
정확도의 경우 long chain PFCAs일수록 낮은 수치를 보였는데 이는 고체상 추출법을 사용한 여러 선행연구에서도 마찬가지로 나타나는 것이 확인되었다[23, 24]. Taniyasu et al. (2005)은 전처리에 사용한 카트리지를 메탄올로 재추출하여 LC-MSMS로 분석한 결과 해당 물질이 10-30% 잔류하고 있음을 확인하였다. 이를 바탕으로 long chain PFCAs가 카트리지 외장재의 구성 물질인 폴리프로필렌에 강하게 흡착하는 성질로 인해 회수율이 다소 낮은 것으로 추측된다[25].
따라서 본 연구에서는 실제 폐수시료에서의 방법검출한계 및 정량한계를 구하기 위해 method 2를 사용하여 폐수 시료 500 mL에 2.5 ng의 혼합표준물질을 주입하여 반복 실험하였다. 혼합표준물질을 주입하지 않은 동일한 시료의 분석을 동시에 실시, 잔류 과불화화합물의 농도를 구하여 그 차이를 이용하여 방법검출한계와 정량한계를 계산하였다. 그 결과, 방법검출한계는 0.17-2.14 ng/L(Table 4), 정량한계는 0.54-6.80 ng/L로 확인되었다.
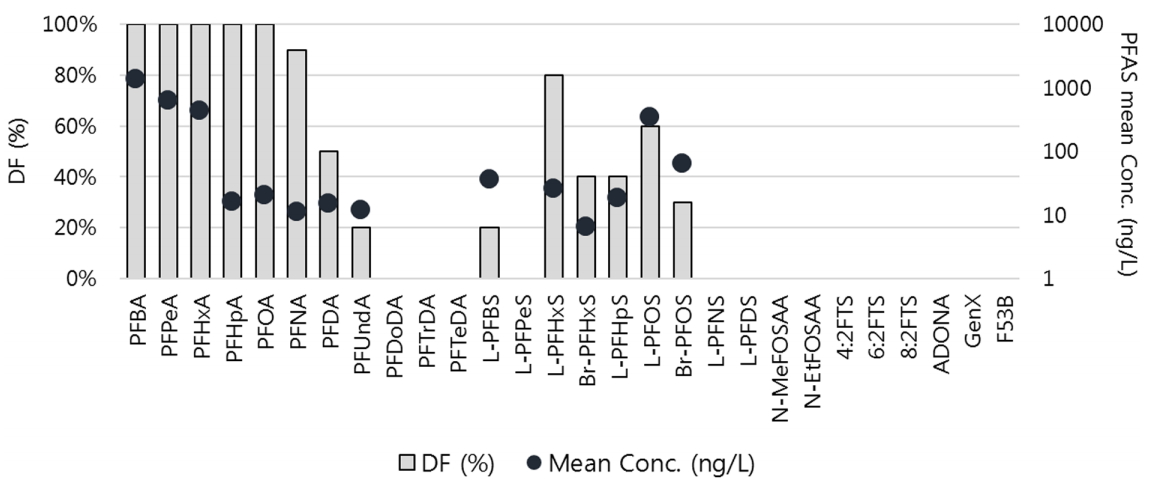
본 연구에서 확인한 적절한 전처리법을 10개의 하, 폐수 시료에 적용하여 PFASs를 분석하였으며 각 물질별 검출 빈도 및 평균 농도를 Fig. 3에 나타내었다. 최초 분석 결과 검정곡선을 초과한 물질의 경우 해당 물질의 농도 수준에 따라 검정곡선 범위에 포함되도록 시료량을 조절하여 재분석하여 농도를 제시하였다. 분석한 시료에서의 총 과불화화합물 농도의 합은 128.4-13,810 ng/L로 검출되었다. 조사된 28종의 과불화화합물 중에서 총 14종의 과불화화합물이 검출되었으며 이 중 2개 물질이 30% 미만의 검출 빈도로 검출되었다 (PFUnDA, L-PFBS). 또한 long chain PFCAs 및 PFSAs에 속하는 PFDoDA, PFTrDA, PFTeDA, L-PFNS, L-PFDS와 precursor에 속하는 N-MeFOSAA, N-EtFOSAA, 4:2 FTS, 6:2 FTS, 8:2 FTS 그리고 PFOA, PFOS의 대체제인 ADONA, GenX, F53B는 검출 한계 미만인 것으로 확인되었다. PFBA가 평균 농도 1,377 ng/L로 가장 높게 검출되었으며 그 다음으로 PFPeA (평균: 633.6 ng/L), PFHxA (434.1 ng/L) 순으로 alkyl chain 이 상대적으로 작은 short chain PFCAs가 전반적으로 높게 검출되는 경향을 보였다. 유사하게 short chain PFCA (C4-C7 PFCA)가 공단 인근 하천수에서 우세하게 검출되는 경향은 선행연구에서도 확인되었다[29].
뿐만 아니라, 국내 잔류성유기오염물질 공정시험법의 대상 물질에 포함되어 있지 않은 L-PFHpS, br-PFHxS, br-PFOS가 30% 이상의 검출 빈도로 각각 평균 농도 18.5 ng/L, 6.5 ng/L, 63.5 ng/L의 수준으로 검출되었다. L-PFHpS의 경우 국내산업하수처리장에서 ND-2.6 ng/L의 범위로 검출된 결과와 국외산업하수처리장에서 ND-0.3 ng/L로 검출된 결과와 비교하였을 때[30,31], 유사한 수준으로 검출된 것으로 확인되었다. 또한 스페인의 하수처리장에서 최근 수행된 연구는 본 연구 결과와 유 사하게 ND-22.2 ng/L로 검출된 것을 확인하였다[32].
본 연구에서는 PFOS와 PFOA의 대체제로 사용되고 있는 3종의 PFASs 대체물질을 포함한 총 28종의 PFASs를 동시 분석 할 수 있는 분석법을 확립하고, 이를 실제 국내 하, 폐수 시료에 적용하였다. 기존의 폐수 시료 내 과불화화합물 공정시험법(method 1)과 기존 연구를 참고하여 공정시험법 전처리 방법을 수정한 방법(method 2)을 테스트한 결과 두 방법 모두 잔류성 유기오염물질 공정시험법 회수율 기준을 만족하였으나, method 2가 모든 분석대상물질에서 정확도와 정밀도가 short-chain PFAS (PFBA), long-chain PFAS (PFDS), 신종과불화화합물(GenX, ADONA)을 분석하기에 기존 공정시험법보다 상대적으로 적합한 전처리법임을 확인하였다. Method 2를 사용하여 방법검출한계 (0.17~2.14 ng/L)를 확인하였으며, 국내 산업 폐수시료 10개를 대상으로 총 28종의 과불화화합물을 분석하였다. 조사대상 폐수 시료 분석 결과, 28종의 과불화화합물 중에서 총 14종의 과불화화합물이 검출되었으며 PFCA계열 PFBA (C4)부터 PFUndA (C11)까지, PFSA 중 PFBS (C4), L-, Br-PFHxS, (C6), 홀수계 PFSA인 PFHpS (C7), L-, Br-PFOS (C8)가 시료에서 검출되었다. 폐수시료에서 GenX, ADONA, F53B와 같은 신종 과불화화합물과 5종 전구체는 검출되지 않았으나 2018년 낙동강 유역의 정수장 과불화화합물 검출 사례와 신종 과불화화합물의 검출 사례가 국외에서 보고되고 있어 향후 국내에서도 규제대상 물질의 대체 물질이 사용 되어 수환경에서 검출 될 가능성이 있을 것으로 예상된다. 따라서 본 연구를 통해 확립한 분석방법을 이용하여 향 후 국내 수환경에서 과불화화합물 대체제를 비롯한 신종 과불화화합물의 지속적인 모니터링이 가능할 것으로 사료된다.
Fig. 1.
Pretreatment methods for the analysis of 28 poly- and per-fluoroalkyl substances (PFASs) in wastewater samples (Method 1: Korean standard analytical method for POPs, (2017), Method 2; modified Korean analytical method for POPs based on Taniyasu et al. (2005))
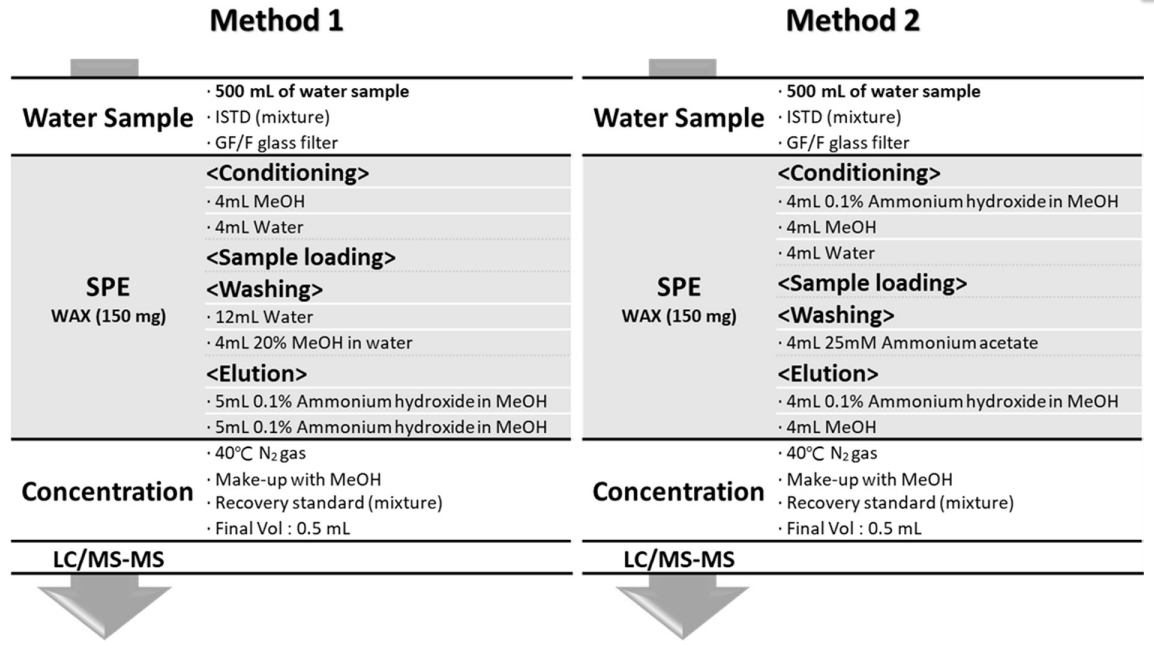
Fig. 2.
Recovery percentage (mean ± standard deviation) of PFAS internal standards from wastewater samples using two different methods (Method 1: Korean standard operating procedure for POPs, (2017), Method 2: Taniyasu et al. (2005))

Table 1.
Target poly- and per-fluoroalkyl substances (PFASs) selected in this study (n = 28) using the Korean standard analytical method for persistent organic pollutants (POPs) (2017) (n = 14)
Table 2.
Liquid chromatography-tandem mass spectrometry (LC-MS/MS) conditions for PFASs analysis
Table 3.
Retention time, precursor ion, and quantification/qualification ion for the target PFASs compounds
Table 4.
Method accuracy and precision for the extraction of PFAS in wastewater samples (Method 1: Korean standard analytical method for POPs, 2017; Method 2: modified analytical method for POPs, 2005)
Table 5.
Method detection limits (MDL) and limits of quantification (LOQ) of PFASs in wastewater samples (unit: ng/L)
참고문헌
1. K. Prevedouros, I. T. Cousins, R. C. Buck, and S. H. Korzeniowski, “Sources, fate and transport of perfluorocarboxylates”, Environmental science and technology, 2006, 40, 32-44.


2. C. P. Higgins, and R. G. Luthy, “Sorption of perfluorinated surfactants on sediments”, Environmental science and technology, 2006, 40, 7251-7256.


3. 식품의약품안전평가원, 과불화옥탄산(PFOA) 및 과불화 옥탄술폰산(PFOS) 위해평가, 2015, 제1판.
4. UNEP, “The conference of the parties 4 of the Stockholm Convention (COP-4) in Geneva placed perfluorooctane sulfonate and perfluorooctane sulfonyl fluoride (PFOS and PFOSF)”, http://chm.pops.int/, February, 2009
5. UNEP, “SC-9/12: Listing of perfluorooctanoic acid (PFOA), its salts and PFOA-related compounds”, http://chm.pops.int/, June, 2019
6. UNEP, “POPRC-15/1: Perfluorohexane sulfonic acid (PFHxS), its salts and PFHxS-related compounds”, http://chm.pops.int/, October, 2019
7. ECHA, “Amending Annex XVII to Regulation (EC) No 1907/2006 of the European Parliament and of the Council concerning the Registration, Evaluation, Authorisation and Restriction of Chemicals (REACH) as regards perfluorooctanoic acid (PFOA), its salts and PFOArelated substances”, https://eur-lex.europa.eu/, June, 2017
8. US Environmental protection agency, “EPA's Per- and Polyfluoroalkyl Substances (PFAS) Action Plan”, https://www.epa.gov/pfas/epas-pfas-action-plan, February, 2019
11. L. S. Birnbaum, and P. Grandjean, “Alternatives to PFASs: perspectives on the science”, Environ Health Perspect, 2015, 123, A104-A105.



12. Z. Wang, J. C. DeWitt, C. P. Higgins, and I. T. Cousins, “A Never-Ending Story of Per- and Polyfluoroalkyl Substances (PFASs)?” Environmental Science & Technology, 2017, 51, 2508-2518.


13. Z. Wang, I. T. Cousins, M. Scheringer, and K. Hungerbuehler, “Hazard assessment of fluorinated alternatives to long-chain perfluoroalkyl acids (PFAAs) and their precursors: status quo, ongoing challenges and possible solutions”, Environment international, 2015, 75, 172-179.


14. G. Munoz, J. Liu, J. S. V. Duy, and S. Sauvé, “Analysis of F-53B, Gen-X, ADONA, and emerging fluoroalkylether substances in environmental and biomonitoring samples: A review”, Trends in Environmental Analytical Chemistry, 2019, e00066.

15. S. Wang, J. Huang, Y. Yang, Y. Hui, Y. Y. Ge, T. Larssen, G. Yu, S. Deng, B. Wang, and C. Harman, “First report of a Chinese PFOS alternative overlooked for 30 years: its toxicity, persistence, and presence in the environment”, Environmental science and technology, 2013, 47, 10163-10170.


16. M. Strynar, S. Dagnino, R. McMahen, S. Liang, A. Lindstrom, E. Andersen, L. McMillan, M. Thurman, I. Ferrer, and C. Ball, “Identification of Novel Perfluoroalkyl Ether Carboxylic Acids (PFECAs) and Sulfonic Acids (PFESAs) in Natural Waters Using Accurate Mass Time-of-Flight Mass Spectrometry (TOFMS)”, Environmental Science and Technology, 2015, 49, 11622-11630.


17. W. A. Gebbink, L. van Asseldonk, and S. P. J. van Leeuwen, “Presence of Emerging Per- and Polyfluoroalkyl Substances (PFASs) in River and Drinking Water near a Fluorochemical Production Plant in the Netherlands”, Environmental Science and Technology, 2017, 51, 11057-11065.


18. A. Jahnke, and U. Berger, “Trace analysis of per-and polyfluorinated alkyl substances in various matrices— how do current methods perform?” Journal of Chromatography A, 2009, 1216, 410-421.


19. M. Petrovic, M. Farré, M. L. De Alda, S. Perez, C. Postigo, M. Köck, J. Radjenovic, M. Gros, and D. Barcelo, “Recent trends in the liquid chromatography-mass spectrometry analysis of organic contaminants in environmental samples”, Journal of Chromatography A, 2010, 1217, 4004-4017.


22. US Environmental protection agency, “Method 537.1 Determination of Selected Per- and Polyflourinated Alkyl Substances in Drinking Water by Solid Phase Extraction and Liquid Chromatography/Tandem Mass Spectrometry (LC/MS/MS)”, http://www.epa.gov, March, 2020
23. S. Taniyasu, K. Kannan, M. K. So, A. Gulkowska, E. Sinclair, T. Okazawa, and N. Yamashita, “Analysis of fluorotelomer alcohols, fluorotelomer acids, and shortand long-chain perfluorinated acids in water and biota”, Journal of Chromatography A, 2005, 1093, 89-97.


24. C. J. Young, V. I. Furdui, J. Franklin, R. M. Koerner, D. C. Muir, and S. A. Mabury, “Perfluorinated acids in arctic snow: new evidence for atmospheric formation”, Environmental science and technology, 2007, 41, 3455-3461.


25. 응선 이, 희영 김, 원진 심, 지현 이, 정은 오, and 형식 김, “혈액과 모유 시료 중 과불화화합물 분석을 위한 전처리법 평가”, 한국환경분석학회지, 2011, 14, 45-54.
26. 재원 최, 정희 김, 용연 김, and 팔진 정, “SPE-LC-MS/MS 에 의한 과불화화합물의 수질분석-고상추출법 비교를 중심으로”, 한국환경분석학회지, 2008, 11, 222-231.
27. J. W. Martin, K. Kannan, U. Berger, P. D. Voogt, J. Field, J. Franklin, J. P. Giesy, T. Harner, D. C. Muir, and B. Scott, “Peer reviewed: analytical challenges hamper perfluoroalkyl research”, Environmental science and technology, 2004, 38, 248A-255A.


28. N. Yamashita, K. Kannan, S. Taniyasu, Y. Horii, T. Okazawa, G. Petrick, and T. Gamo, “Analysis of perfluorinated acids at parts-per-quadrillion levels in seawater using liquid chromatography-tandem mass spectrometry”, Environmental science and technology, 2004, 38, 5522-5528.


29. P. Wang, Y. Lu, T. Wang, Z. Zhu, Q. Li, J. Meng, H. Su, A. C. Johnson, and A. J. Sweetman, “Coupled production and emission of short chain perfluoroalkyl acids from a fast developing fluorochemical industry: Evidence from yearly and seasonal monitoring in Daling River Basin, China”, Environmental Pollution, 2016, 218, 1234-1244.


30. L. Ahrens, S. Felizeter, R. Sturm, Z. Xie, and R. Ebinghaus, “Polyfluorinated compounds in waste water treatment plant effluents and surface waters along the River Elbe, Germany”, Marine pollution bulletin, 2009, 58, 1326-1333.


- TOOLS
-
METRICS

-
- 1 Crossref
- 4,492 View
- 121 Download
-
Related articles in
J Environ Anal Health Toxicol -
Comparison of Pretreatment Methods for the Analysis of PCBs in Transformer Oil2010 September;13(3)